
《最新二类医疗器械备案,是否采用新目录?解析最新政策与操作指南》
二类医疗器械备案是否使用新目录
引言
随着医疗器械行业的迅速发展,为了加强医疗器械的监管和规范化管理,国家对医疗器械进行了分类管理。二类医疗器械备案的问题引起了众多利益相关者的关注。其中,大家最关心的问题之一是:二类医疗器械备案是否使用新目录。本文将详细解析这一问题。

一、二类医疗器械概述
首先,我们需要了解二类医疗器械的定义和范围。二类医疗器械通常是指具有一定的风险性,需要在专业人员的操作下使用,以确保其安全和有效性的医疗设备。这类器械的备案和管理对于保障公众健康至关重要。
二、备案与目录的关系
关于二类医疗器械备案是否使用新目录的问题,答案取决于国家相关部门的政策更新和发布情况。医疗器械的备案目录是监管部门根据行业发展和监管需要进行更新和调整的。因此,备案时应当参照最新的目录版本。
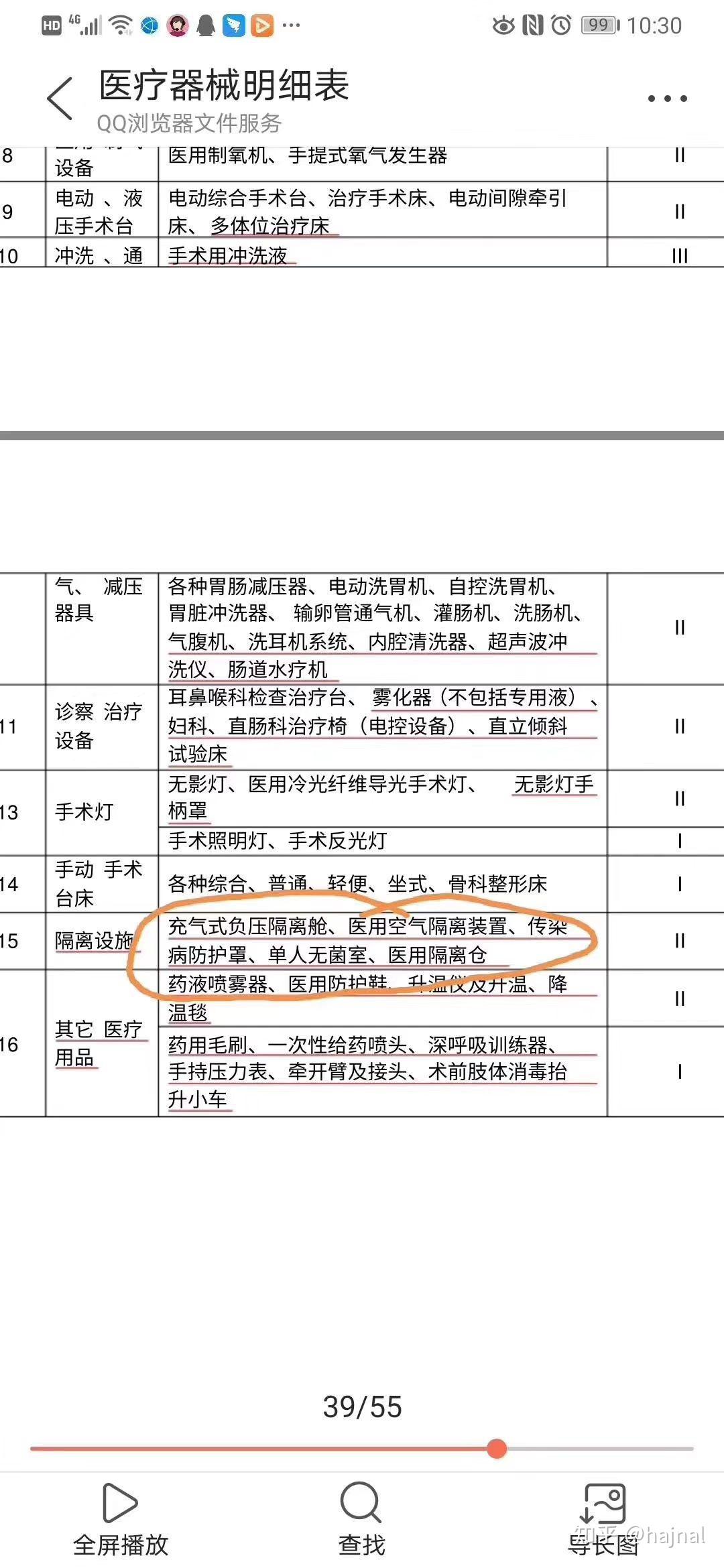
三、新目录的重要性
使用新目录对于备案过程至关重要。新目录通常反映了最新的监管要求和行业标准,确保备案的医疗器械符合国家的安全和质量标准。此外,新目录还有助于提高备案的透明度和公正性。
四、如何获取和使用新目录
为了获取最新的二类医疗器械备案目录,相关单位和个人应及时关注国家相关部门的官方网站,以便获取最新的政策更新和目录信息。在使用新目录时,应确保理解目录中的各项要求和标准,确保备案的准确性和合规性。
结语
总的来说,二类医疗器械备案是否使用新目录取决于最新政策的发布和实施情况。相关单位和个人应密切关注政策动态,确保备案工作的准确性和合规性。只有这样,才能保障公众的健康和安全。































